육종인·황금숙 연구팀, 특정 단백질 활용 대사 억제 과정 규명
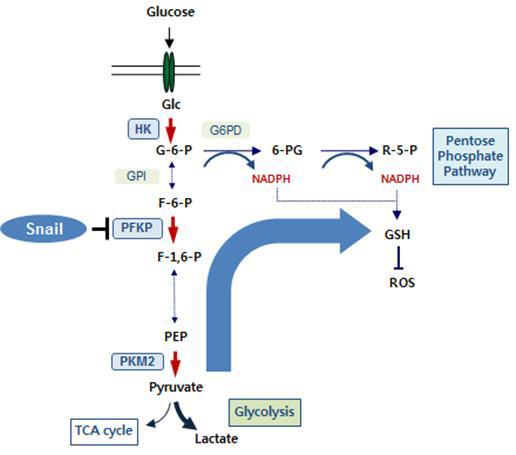
연구팀은 암세포가 주변 조직을 공격하여 뻗어나가고(침윤), 처음 발생한 장기로부터 혈관, 림프관을 타고 다른 조직으로 퍼져나가는(전이) 것은 암세포 스스로 특정 단백질(스네일)을 이용해 대사물질(PFKP)을 억제해 대사를 조절함으로써 이뤄진다는 것을 최초로 밝혔다.
스네일은 발생과정 및 암의 진행과정에서 세포와 세포 사이 부착물질인 카데린(E-cadherin)의 전사를 억제해 상피간엽이행을 유도, 세포부착의 소실, 세포골격의 변화 및 운동성의 획득에 관여하는 단백질이다.
전이 과정의 암세포에서는 스네일이 당대사경로에서 호기성 해당작용과 5탄당 인산경로의 스위치 역할을 하는 대사물질을 억제시켜, 암세포가 생존할 수 있는 환원력을 얻는다는 사실을 발견했다.
전이 암세포가 대사 조절의 핵심 물질로 이용한 것이 PFKP라는 것은 동물실험에서도 확인됐다. 동물 전이 모델에서 암유전자인 스네일은 폐 전이를 증가시키고, 여기에 PFKP를 증가시키면 다시 폐 전이가 억제됐다. 이는 스네일이 PFKP 발현을 억제해 암세포의 생존능력을 증가시켜 생체 내에서 암 전이를 유도함을 보여주는 결과라고 연구팀은 설명했다.
육종인 교수는"이번 연구성과는 그 동안 연구가 전무했던 전이 과정의 암세포 대사 조절에 대한 최초의 연구보고이다. 6년의 오랜 연구 끝에 전이되는 암세포는 증식하는 암세포와 달리 이화작용 쪽으로 대사를 조절하여 생존하게 한다는 것을 밝혔다"며 "새로운 대사 치료표적을 제공함으로써 대사경로의 타깃이 알려져 있는 기존 대사약제를 암 치료에 적용할 수 있는 근거를 제공할 것으로 기대된다"고 말했다.
이 연구성과는 미래창조과학부·한국연구재단의 기초연구사업(개인연구), 교육부·한국연구재단의 학문후속세대양성지원사업의 지원을 받아 수행됐다. 국제 학술지 네이처 커뮤니케이션즈(Nature Communications) 지난달 8일자에 게재됐다.
김달호 기자
<저작권자ⓒ대전일보사. 무단전재-재배포 금지>
